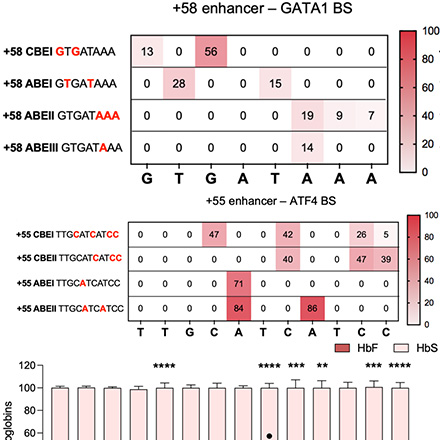
بیماری گلبول قرمز داسی شکل یا Sickle Cell Disease (SCD) یک بیماری ارثی اتوزومی مغلوب است. این بیماری معمولا در اثر یک جهش نقطه ای در ژن بتا گلوبین ایجاد شده و باعث ایجاد فنوتیپ داسی شکل گلبول های قرمز میشود.
از علائم این بیماری میتوان به کم خونی شدید، بزرگی طحال، تنگی نفس و درد قفسه سینه اشاره کرد. درد های ناگهانی قفسه سینه، شکم، دست ها و یا پاها در این بیماران (vaso-occlusive pain crisis) در اثر مسدود شدن رگ های خونی به علت شکل غیر طبیعی گلبول های قرمز و چسبندگی آنها، اتفاق میافتد.
افراد مبتلا به این بیماری ژنتیکی، مجبور به دریافت دارو هایی مانند Hydroxyurea و یا دریافت خون با توجه به شدت بیماری، در تمام طول زندگی خود هستند.
ژن درمانی، خصوصا ژن درمانی برپایه فناوری کریسپر، امید تازه ای برای درمان قطعی بیماران SCD و Thalassemia ایجاد کرده است.
در پژوهشی که به تازگی در Cell Reports Medicine منتشر شده است، با بررسی مناطق قابل هدفگیری توسط ویرایشگر های باز، به بررسی میزان تاثیر ناحیه ویرایش، تاثیر نوع ویرایشگر باز استفاده شده و مقایسه آن با ویرایش توسط Cas9 پرداخته شده است. در این پژوهش با ایجاد تغییر در توالی های محل اتصال GATA1 و ATF4 در BCL11a enhancer regions، میزان تولید بتا گلوبین معیوب را کاهش و باعث جایگیزی آن با گلوبین جنینی شده اند. روش جایگزینی گلوبین جنینی با بتا گلوبین معیوب، برای سایر بیماری های مختلف خونی که در آن زیرواحد بتا دچار اختلال شده (مانند تالاسمی) نیز کار آمد است. در این پژوهش نشان داده شده است که با کمک ویرایشگر های باز امکان ویرایش و افزایش بیان هموگلوبین جنینی وجود دارد اما میزان بیان هموگلوبین جنینی، در حالتی که از Cas9 و gRNA ای که ناحیه +۵۸ را هدف قرار میدهد، بیشتر است. این افزایش بیان گلوبین جنینی با ایجاد Indel های متفاوت در ناحیه هدف توسط Cas9 اتفاق می افتد اما در ویرایش باز شاهد میزان بسیار کمی از indel ها هستیم که میتواند باعث حفظ بیشتر پایداری ژنتیکی محل ویرایش شود. در ادامه به Xenotransplantation سلول های بنیادی خون ساز مغز استخوان (HSCs) ویرایش شده به موش NBSGW پرداخته شده و نتایج حاص مقایسه شده اند.
در انتها باید در نظر داشت که ویرایش باز برای درمان تالاسمی و گلبول قرمز داسی شکل وارد کارازمایی بالینی شده و به شکل درون تنی (In Vivo) مورد استفاده قرار گرفته است.
نتایج حاصل از کارآزمایی های بالینی میتواند معیار مناسبی برای ارزیابی توانایی های این ابزار دقیق را برای ژن درمانی باشد.
نویسنده: احمدرضا شاپورزاده
مرجع
https://doi.org/10.1016/j.xcrm.2025.102376
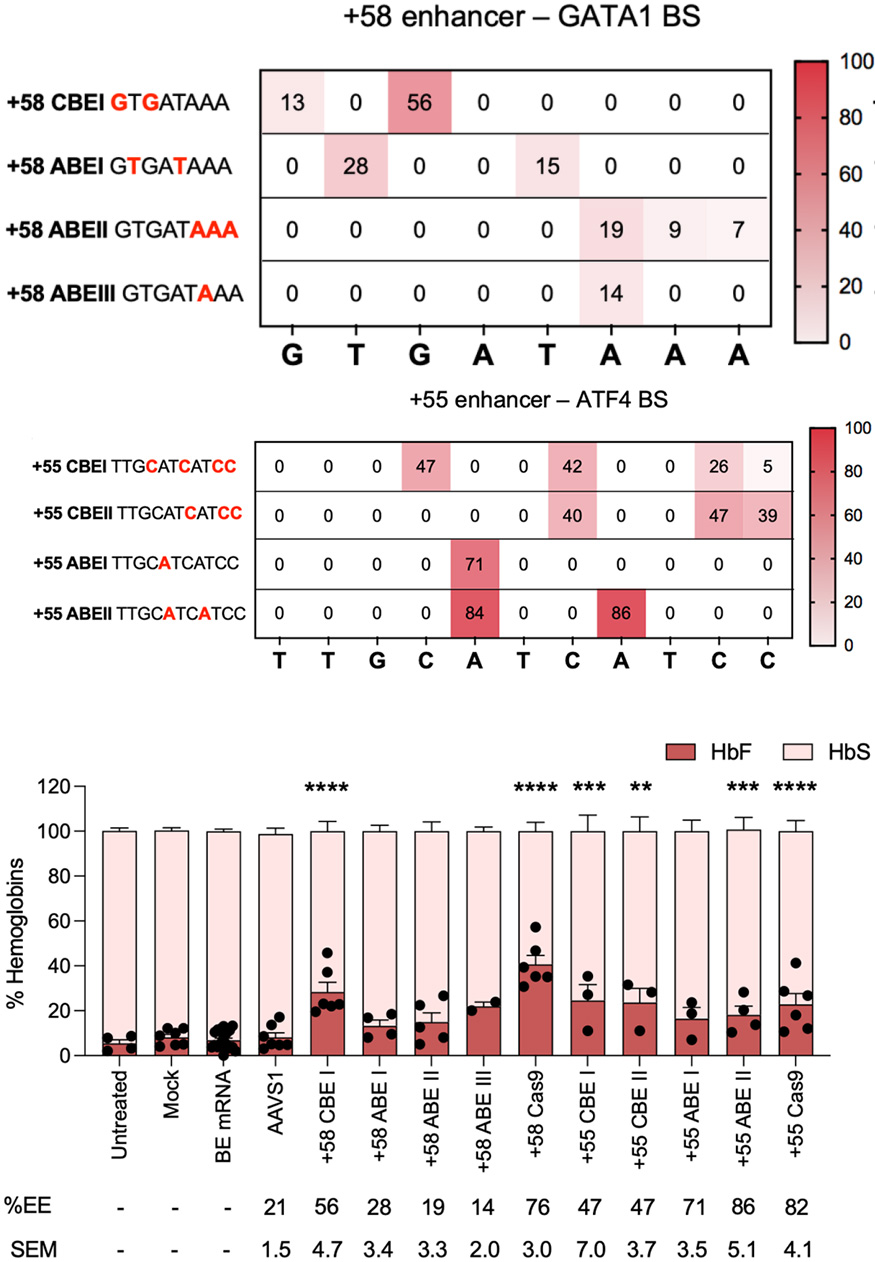
۱: بررسی میزان ویرایش در نواحی مختلف هدف توسط ویرایشگر های باز
2: بررسی میزان HbF و HbS توسط Cation-Exchange HPLC برای سلول های بنیادی ویرایش شده و تمایز یافته به RBC در In Vitro.