در این مطالعه، یک روش نوآورانه و حساس برای تشخیص mRNA ویروس پاپیلومای انسانی با ریسک بالا (hrHPV) ارائه شده است. این روش با استفاده از واکنش زیستشناسی مولکولی RT-RPA (Reverse Transcription Recombinase Polymerase Amplification) قادر است mRNA انواع HPV16، HPV18 و HPV45 را به صورت مستقیم و بدون نیاز به استخراج RNA، از نمونههای بالینی سلولهای دهانه رحم تشخیص دهد.
روش RT-RPA چیست؟
روش RT-RPA یک آزمون ایزوترمال و سریع است که در دمای ثابت حدود ۳۹ درجه سانتیگراد انجام میشود. این روش ترکیبی از دو مرحله است: تبدیل mRNA به DNA مکمل (cDNA) توسط آنزیم reverse transcriptase و سپس تکثیر DNA هدف با استفاده از فرآیند بازترکیبی (Recombinase Polymerase Amplification). این تست به اندازه آزمون مورد تأیید سازمان غذا و دارو آمریکا (FDA)، Aptima حساسیت دارد و توانایی تشخیص حداقل ۱۰۰ نسخه mRNA را در هر واکنش دارد.
نمونهبرداری و آماده سازی نمونه
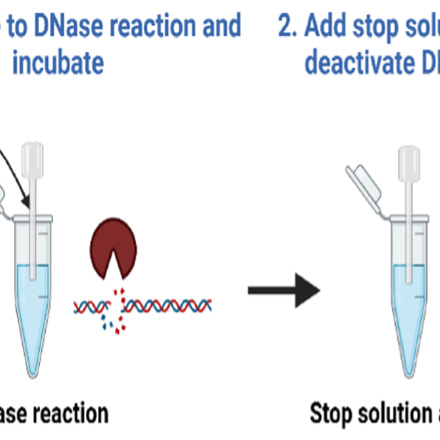
نمونههای بالینی از سلولهای دهانه رحم گرفته میشوند و به جای استخراج پیچیدهRNA، با روشی مستقل از استخراج و تنها با یک واکنش آنزیمی ساده (استفاده از DNase برای حذف DNA سلولی و ویروسی) آماده میشوند. سپس نمونههای آماده شده مستقیماً وارد واکنش RT-RPA میشوند که با استفاده از فلوریمتر قابل حمل، نتایج آنی در کمتر از ۲۰ دقیقه ارائه میشود.
مزایای این روش
- حساسیت و اختصاصیت بالا: آزمون RT-RPA طراحی شده قادر است به طور دقیق و اختصاصی mRNA پروتئینهای E7 ویروس HPV را تشخیص دهد بدون تشخیص غیرهدف یا آلوده شدن به DNA ویروس.
- سرعت بالا: نتایج سریع در کمتر از ۱۵ دقیقه برای RNA استخراج شده و ۲۰ دقیقه برای نمونههای خام.
- سادگی و هزینه پایین: حذف نیاز به استخراج پیچیده RNA، تجهیزات گرانقیمت و نیروی متخصص آزمایشگاهی، موجب میشود این روش برای آزمایشهای میدانی و محیطهای با منابع محدود بسیار مناسب باشد.
- کنترل داخلی قابل اطمینان: اضافه کردن بررسی mRNA ژن β-actin به عنوان کنترل سلولی، کیفیت نمونه و صحت تست را تأیید میکند.
توسعه و بهینهسازی تکنیکی
- پرایمرها و پروبهای خاص برای انواع HPV طراحی و بهینه شده تا بیشترین حساسیت را داشته باشند.
- به کارگیری آنزیم Omniscript به عنوان بهترین reverse transcriptase برای پیشآمادهسازی واکنش.
- استفاده از توپک فلزی مغناطیسی برای مخلوط شدن یکنواخت واکنش به دلیل ویسکوزیته بالای محیط RPA.
نتایج بالینی
در آزمایش بر روی ۱۱ نمونه بالینی، نتایج RT-RPA با نتایج استاندارد طلایی RT-qPCR کاملاً مطابقت داشت. این روش توانست به طور اختصاصی و حساس mRNA انواع ویروسهای HPV را در نمونههای بالینی از سلولهای دهانه رحم شناسایی کند.
چشمانداز آینده
- گسترش این آزمون برای شناسایی سایر انواع خطرناک HPV برای بهبود تشخیص بالینی.
- توسعه فرمهای خشک (لیوفیلیزه) واکنش برای پایداری ذخیره و حمل و نقل در محیطهای با منابع محدود.
- کاهش هزینهها با استفاده از واکنشهای دوگانه مولتیپلکس و جایگزینی تجهیزات تجاری با نمونههای متنباز.
مرجع
https://doi.org/10.1038/s41598-025-13583-2