درمانهای مبتنی بر RNA پیامرسان (mRNA), که در قالب نانوذرات لیپیدی (LNPs) فرموله میشوند، بهعنوان یکی از فناوریهای تحولآفرین در زمینههایی چون واکسنسازی، ایمنیدرمانی، جایگزینی پروتئین و ویرایش ژن مطرح شدهاند. با این حال، یکی از چالشهای اساسی در استفاده از آنها، نبود روشهای کارآمد برای رسانش اختصاصی به سلولهای هدف است؛ موضوعی که بر اثربخشی و ایمنی این درمانها تأثیر مستقیم دارد.
mRNA قادر است درون سلولهای هدف ترجمه شده و پروتئینهای درمانی یا آنتیژنی را تولید کند، بدون اینکه نیاز به وارد کردن DNA یا تغییرات ژنتیکی پایدار داشته باشد. با این حال، چالش اصلی در درمانهای مبتنی بر mRNA، رسانش مؤثر و اختصاصی آن به سلولهای مورد نظر است mRNA مولکولی ناپایدار است و در محیط بدن بهسرعت توسط ریبونوکلئازها تجزیه میشود. به همین دلیل، برای محافظت و انتقال آن، از نانوحاملهایی نظیر نانوذرات لیپیدی (Lipid Nanoparticles; LNPs) استفاده میشود. در این مطالعه، سامانهای نوین از نانوذرات لیپیدی توسعه داده شد که قابلیت هدفگیری اختصاصی سلولی را داراست. برای این منظور، سطح نانوذرات با نانوبادیهای (VHH) اختصاصی علیه آمینوپپتیداز N (APN) ــ یک پروتئین غشایی موجود در سلولهای اپیتلیال روده ــ پوشانده شد. این نانوبادیها در باکتری E. coli مهندسیشده ژنتیکی تولید شدند تا اسیدآمینهی غیرطبیعی آزیدو_ فنیلآلانین در ساختارشان گنجانده شود. وجود این گروه شیمیایی امکان اتصال دقیق و کنترلشدهی نانوبادیها به نانوذرات لیپیدی حاوی DSPE-PEG2000-TCO را از طریق واکنش دو مرحلهای شیمی کلیک (SPAAC) و (IEDDA) فراهم کرد.
یافتهها نشان دادند که نانوذرات هدفمندشده با نانوبادی ضد-APN، بهصورت انتخابی به سلولهای بیانکنندهی APN متصل شده و آنها را بهطور مؤثری درونگیری میکنند. این امر منجر به افزایش جذب نانوذرات و انتقال کارآمدتر mRNA به داخل سلولها شد. افزون بر این، هدایت نانوذرات mRNAدار مجهز به نانوبادی به سوی گیرندهی APN موجب عبور مؤثر آنها از سد اپیتلیال روده گردید؛ نتایجی که در مدلهای انداموارهای روده خوک و آزمایشهای درونتنی تأیید شدند.
بهطور کلی، این پژوهش پلتفرمی نوآورانه و قابل برنامهریزی را برای رسانش اختصاصی mRNA معرفی میکند که میتواند در توسعهی واکسنها و درمانهای مبتنی بر RNA با هدفگیری دقیق سلولی مورد استفاده قرار گیرد. اگرچه تمرکز این مطالعه بر APN در خوک بود، روش بهکاررفته بهراحتی قابل تطبیق برای گونهها و اهداف دیگر است و چشماندازی نو برای درمانهای mRNA فراهم میسازد.
نویسنده: ساناز صدقی اصفهانی
مرجع
https://doi.org/10.1016/j.jconrel.2025.114365

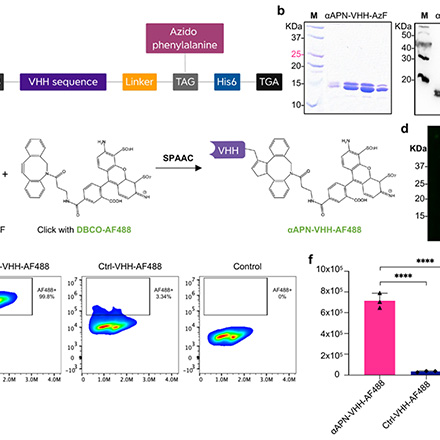
تولید آنتیبادیهای تکدامنهای ضد APN اصلاحشده با پارا-آزیدو فنیلآلانین
(a) طراحی نانوبادی اختصاصی APN (αAPN-VHH-AzF) که شامل اسید آمینه آزیدو-فنیلآلانین در ساختار خود است.
(b) رنگآمیزی کوماسی (سمت چپ) و وسترن بلات اختصاصی برای VHH سمت راست که حضور و خلوص αAPN-VHH-AzF تصفیهشده از دستههای مختلف را نشان میدهد. (۱۰ میکرولیتر از هر نمونه بارگذاری شده است).
(c) نمودار شماتیک واکنش اتصال حلقوی آزید-آلکین تقویتشده با کشش (SPAAC) بین نانوبادی دارای گروه آزید VHH-AzF و ترکیب DBCO-AF488، که منجر به تشکیل VHH-AF488 از طریق یک راهبرد اتصال تکمرحلهای میشود.
(d) (ژل SDS-PAGE فلورسنت (در کانال AF488 تأیید میکند که برچسبگذاری نانوبادی با رنگ AF488 با موفقیت انجام شده است. در هر مسیر ژل، ۱ میکروگرم از VHH-AF488 بارگذاری شده است.
نمودارهای فلوسایتومتری نماینده که اتصال αAPN-AF488 و Ctrl-VHH-AF488 را به سلولهای BHK-APN پس از ۱ ساعت انکوباسیون در دمای ۴ درجه سانتیگراد نشان میدهد. ترکیبات اتصالیافته با استفاده از شیمی کلیک یکمرحلهای یا دومرحلهای تهیه شدهاند.
(f) تحلیل کمی فلوسایتومتری از اتصال به APN. دادهها بهصورت میانگین ± انحراف معیار از سه دسته مستقل (n = 3) از αAPN-VHH-AzF ارائه شدهاند. دادهها با آزمون آماری ANOVA یکطرفه تحلیل شدند. علامت **** نشاندهندهٔ p < 0.0001 است.
:Mنشانگر وزن مولکولی.