نویسنده: امیرمحمد محمدی آرا
اینترلوکین-۲۱ (IL-21) یکی از سایتوکینهای کلیدی سیستم ایمنی تطبیقی است که اثرات گستردهای بر لنفوسیتهایT، سلولهای B و سلولهای NK اعمال میکند. این مولکول، عمدتاً توسط سلولهای T فولیکولار هلپر (Tfh) و سلولهای T CD4+ تولید میشود و تعادل بین پاسخهای التهابی و سرکوب ایمنی را تنظیم مینماید. در ایمونوتراپی سرطان، IL-21 به عنوان عاملی امیدبخش عمل میکند، زیرا پاسخهای ضدتوموری را بدون ایجاد سرکوب ایمنی گسترده تقویت مینماید. چالش اصلی، فعالسازی سلولهای T سایتوتوکسیک (CD8+) با دامنه وسیعی از تمایلات پیوندی به آنتیژنهای توموری است، در حالی که مهار توسط سلولهای T تنظیمی (Treg) به حداقل برسد.
برای غلبه بر محدودیتهای IL-21 طبیعی، مانند نیمهعمر کوتاه و سیگنالدهی ضعیف، محققان شبهمولکول 21h10
را از طریق مهندسی پروتئینی de novo طراحی کردهاند. این مولکول پایداری ساختاری بالایی دارد، نیمهعمر گردش خونی طولانیتری ارائه میدهد و سیگنالدهی قویتری از طریق گیرنده IL-21R در انسان و موش ایجاد میکند. 21h10 واکنش متقاطع کاملی با گیرندههای انسانی و موشی این سایتوکاین دارد، که ارزیابی پیشبالینی را تسهیل مینماید.
در مدلهای ارگانوتیپیک موشی و ex vivo انسانی، 21h10 فعالیت ضدتوموری قدرتمندی بروز میدهد که از نظر مدت زمان و شدت سیگنالدهی، برتر از IL-21 طبیعی است و نفوذ عمیقتر به بافت تومور را ممکن میسازد. درمان با 21h10 حجم تومور را کاهش و بقای حیوانات را افزایش داد، که با ایمونوهیستوشیمی تأیید شده است. با این حال، در موشها پانکراتیت حاد مشاهده گردید، که با مهار TNF-α (مانند اتانرسپت) بدون اختلال در اثربخشی ضدتوموری، کنترل شد. علاوه بر این، علیرغم تشکیل آنتیبادیهای ضددارویی علیه 21h10 در موشها، این آنتیبادیها ماهیت غیرخنثیکننده (non-neutralizing) داشتند؛ در نتیجه، موشها همچنان قادر به پاسخدهی ایمنی به درمانهای بعدی با 21h10 بودند، که این امر پایداری طولانیمدت درمان را تضمین میکند.
یافتههای کلیدی حاکی از القای سلولهای T سایتوتوکسیک با دامنه گسترده تمایلات پیوندی، به ویژه گسترش سلولهای درونتوموری با میل پایین است. نسبت به IL-21 طبیعی، 21h10 بیان IFN-γ و گرانزیم B را به طور چشمگیر افزایش میدهد و فراوانی سلولهای Th1 را بالا میبرد، در حالی که جمعیت Treg را کاهش میدهد، که این امر تعادل ایمنی را به سمت پاسخهای ضدتوموری سوق میدهد.
در نتیجه، ویژگیهای 21h10، از جمله پایداری بالا، توانایی سیگنالدهی بهتر و القای پاسخ در سلولهای T با میل پیوندی پایین، پتانسیل ترجمهای قابلتوجهی را نشان میدهد. این مولکول میتواند پایه درمانهای ترکیبی به ویژه با checkpoint inhibitors مانند anti-PD-1 برای سرطانهای جامد مانند ملانوما یا پانکراس باشد. 21h10 نمادی از پیشرفتهای مهندسی پروتئین در ایمونولوژی سرطان است و امیدواری برای نسل جدیدی از درمانهای شخصیسازیشده را القا میکند.
مرجع
https://doi.org/10.1126/sciimmunol.adx1582
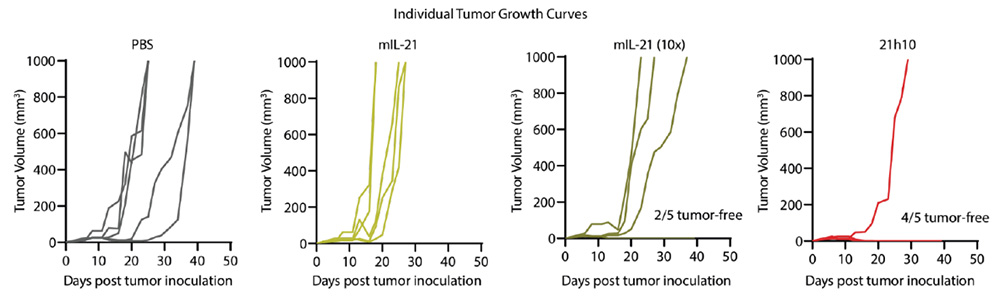
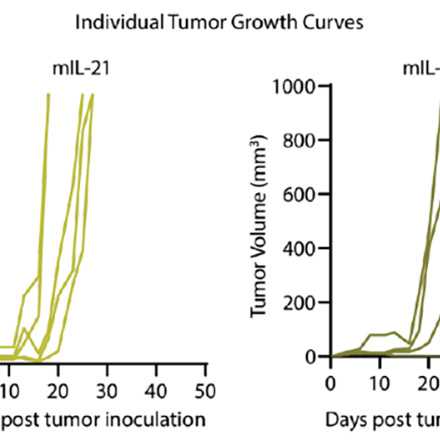
نرخ زندهمانی بیشتر و میزان رشد کمتر تومور در گروه دریافت کننده 21h10 نسبت به گروه دریافت کننده اینترلوکین-۲۱ و گروه کنترل در مدل موشی ملانوما