باوجود نقش پررنگ واکسنهای mRNA در تحولات نوین ایمنیزایی، چالش کلیدی این حوزه هنوز انتقال کارآمد و هدفمند mRNA به سلولهای ایمنی ارائهدهنده آنتیژن، بهویژه سلولهای دندریتیک (DCs) است. یکی از موانع مهم در مسیر کارایی واکسنها، برداشت غیراختصاصی نانوذرات حامل mRNA توسط ماکروفاژها و کاهش دسترسی نانو واکسن به بافتهای لنفاوی و سلولهای هدف بوده است.
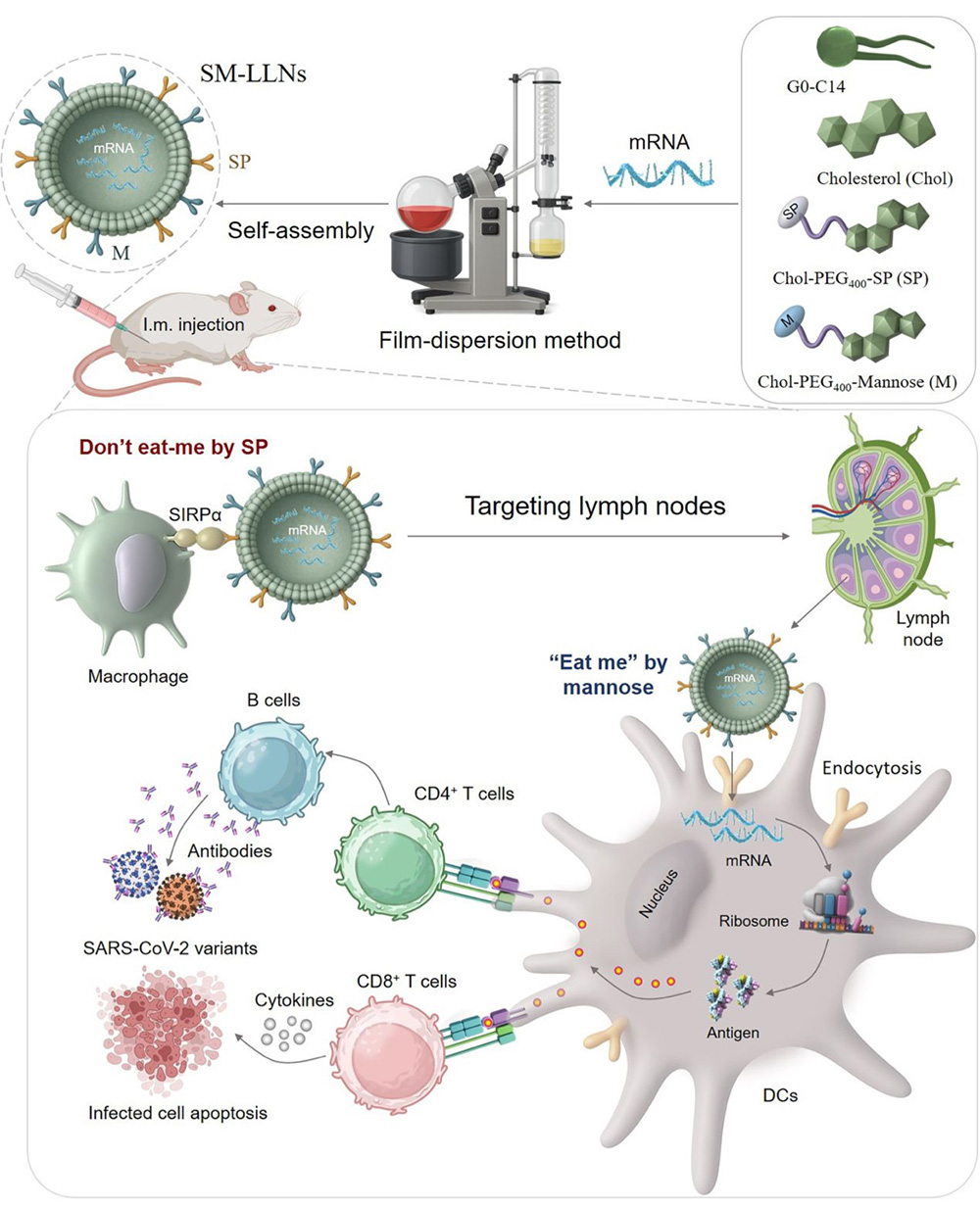
در این پژوهش، محققان سامانهای پیشرفته از نانوذرات شبهلیپیدی (LLNs) تحت عنوان SM-LLNs را طراحی کردهاند که با استفاده همزمان از دو لیگاند خاص (Chol-PEG400-SP و Chol-PEG400-Mannose) هم برداشت توسط ماکروفاژ را محدود میکند و هم جذب اختصاصی توسط سلولهای دندریتیک را افزایش میدهد.
- پپتید مشتق از CD47 (SP)، با ارسال سیگنال بازدارنده به ماکروفاژها و تعامل با گیرنده SIRPα، برداشت غیرهدفمند ذرات را کاهش می دهد.
- لیگاند مانوز ، با هدفگیری گیرندههای مانوز روی سلولهای دندریتیک، جذب اختصاصی و ورود نانوذره به این سلولها را تقویت میکند.
این رویکرد دوگانه موجب افزایش انتقال mRNA به غدد لنفاوی، ارتقاء بلوغ DC، و نهایتاً بهبود ارائه آنتیژن میشود.
نتایج
- کاهش برداشت غیرهدفمند: افزودن پپتیدCD47 باعث شد میزان جذب نانوذره توسط ماکروفاژها بهطور چشمگیری کاهش پیدا کند؛ بهطوری که شدت جذب از حدود ۸۰٬۰۰۰ به ۵۰٬۰۰۰ واحد (MFI) کاهش یافت. این کاهش از نظر آماری کاملاً معنیدار بود و نشان داد که با این تغییر، مقدار ورود نانوذره به سلولهای غیرهدف حدوداً نصف شد.
- افزایش هدفگیری: حضور لیگاند مانوز بر سطح نانوذره، جذب اختصاصی توسط سلولهای دندریتیک را تا سه برابر در مقایسه با سایر گروهها افزایش داد و ارائه آنتیژن را به نحوی چشمگیر بهبود بخشید.
- تقویت بیان ژن و تداوم ایمنی: تزریق عضلانی SM-LLNs حاوی mRNA اسپایک کرونا، بیان بالای پروتئین در عضله و غدد لنفاوی را ایجاد کرد که تا ۲۴ ساعت پایدار ماند.
- پاسخ هومورال قوی: گروه SM-LLNs سطوح قابلتوجهی از آنتیبادی IgG علیه انواع دلتا، اُمیکرون و سویه مرجع (wild-type) کرونا تولید کرد که حداقل تا ۷۰ روز در سطح بالا باقی ماند. تستهای خنثیسازی ویروس (NT50) در این گروه بالاترین مقادیر را نشان داد.
- پاسخ سلولی Th1 هدفمند: بلوغ DC در طحال و غدد لنفاوی و افزایش سلولهای CD4+ و CD8+ تولیدکننده IFN-γ و IL-2 مشهود بود، نشاندهنده گرایش قوی پاسخ ایمنی به سمت محور Th1 که برای پاکسازی ویروس اهمیت کلیدی دارد.
- ایمنی مطلوب: بررسیهای پاتولوژیک و آزمایشات خونی هیچ عارضه قابلتوجهی نشان نداد؛ زیستسازگاری و عدم سمیت سامانه تأیید شد.
شواهد این مطالعه نشان داد که راهبرد هوشمند استفاده همزمان از دو نوع لیگاند در نانوذرات، امکان مقابله با معضل برداشت غیرهدفمند را فراهم کرده و تحویل مؤثر، انتخابی و ایمن mRNA به DCها و بافتهای لنفاوی را تضمین میکند. این رویکرد نه تنها در مقابله با کرونا، بلکه در انواع ایمونوتراپیهای آینده بیماریهای عفونی و سرطان قابل بسط خواهد بود.
نکته کلیدی، اثربخشی و ایمنی بسیار بالای SM-LLNها حتی در دوزهای تکراری و در مدلهای مختلف است که امید بسیاری برای بالین و توسعه نسل آینده واکسنهای هدفمند بر پایه mRNA ایجاد میکند.
مرجع
https://doi.org/10.1016/j.celbio.2025.100180
شرح تصویر: روند ساخت نانو واکسن SM-LLNs و نقش تخصصی دو لیگاند در هدفگیری سلولی: پس از تزریق، نانوذره با کاهش برداشت توسط ماکروفاژ و افزایش جذب توسط سلولهای دندریتیک، موجب انتقال هدفمند mRNA به لنف و تقویت پاسخ ایمنی ضد کرونا میشود.